Luigi Ricciardi 1 , Rosa Mazzeo 2,*©, Angelo Raffaele Marcotrigiano 1 , Guglielmo Rainaldi 3 , Paolo Iovieno 4 , Vito Zonno 1 , Stefano Pavan 1 © e Concetta Lotti 2,*
- 1 Dipartimento di Scienze del Suolo, della Pianta e degli Alimenti, Unità di Genetica Vegetale e Breeding Università degli Studi di Bari, Via Amendola 165/A, 70125 Bari, Italia; luigi.ricciardi@uniba.it (LR);angelo.marcotrigiano@uniba.it (BRACCIO); vito.zonno@uniba.it (VZ); stefano.pavan@uniba.it (SP)
- 2 Dipartimento di Scienze dell'Agricoltura, dell'Alimentazione e dell'Ambiente, Università di Foggia, Via Napoli 25, 71122 Foggia, Italia
- 3 Dipartimento di Bioscienze, Biotecnologie e Biofarmaceutiche, Università degli Studi di Bari, Via Orabona 4, 70125 Bari, Italia; guglielmo.rainaldi@uniba.it
- 4 Dipartimento di Tecnologie Energetiche, Divisione Bioenergia, Bioraffinerie e Chimica Verde, Centro Ricerche ENEA Trisaia, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), Italia; paolo.iovieno@enea.it
* Corrispondenza: rosa.mazzeo@unifg.it (RM); concetta.lotti@unifg.it (CL)
Abstract:
cipolla (Allium cepa L.) è la seconda coltura vegetale più importante al mondo ed è ampiamente apprezzata per i suoi benefici per la salute. Nonostante la sua significativa importanza economica e il suo valore come alimento funzionale, la cipolla è stata scarsamente studiata per quanto riguarda la sua diversità genetica. Qui, abbiamo esaminato la variazione genetica della “cipolla rossa Acquaviva” (ARO), una varietà autoctona con una storia secolare di coltivazione in un piccolo paese della provincia di Bari (Puglia, Sud Italia). Una serie di 11 marcatori microsatelliti è stata utilizzata per esplorare la variazione genetica in una raccolta di germoplasma composta da 13 popolazioni ARO e tre tipi commerciali comuni. Analisi della struttura genetica con metodi parametrici e non parametrici hanno evidenziato che l'ARO rappresenta un pool genetico ben definito, chiaramente distinto dalle varietà autoctone di Tropea e Montoro con le quali viene spesso confuso. Al fine di fornire una descrizione dei bulbi, solitamente utilizzati per il consumo fresco, sono stati valutati il contenuto di solidi solubili e il piccante, mostrando una maggiore dolcezza nell'ARO rispetto alle due varietà autoctone sopra menzionate. Nel complesso, il presente studio è utile per la futura valorizzazione dell'ARO, che potrebbe essere promossa attraverso marchi di qualità che potrebbero contribuire a limitare le frodi commerciali e migliorare il reddito dei piccoli proprietari terrieri.
Introduzione
Il genere Allium comprende circa 750 specie [1], tra cui la cipolla (Allium cepa L., 2n = 2x =16) è una delle più diffuse. A. cepa ha un ciclo biennale e un comportamento riproduttivo incrociato. Al giorno d’oggi, la produzione globale di cipolla (97.9 Mt) la rende la seconda coltura vegetale più importante dopo il pomodoro [2]. Fin dall'antichità i bulbi delle cipolle venivano utilizzati sia come alimento che in applicazioni medicinali popolari. Già gli antichi Egizi, infatti, riportavano diverse formule terapeutiche basate sull'uso di aglio e cipolla in un papiro medico del 1550 aC, il Codex Ebers [3].
Questo ortaggio versatile e salutare viene consumato crudo, fresco o come prodotto trasformato, e utilizzato per esaltare il gusto di moltissimi piatti. Diversi studi recenti affermano che il consumo di cipolla può ridurre il rischio di malattie cardiovascolari [4,5], obesità [6], diabete [7] e varie forme di cancro [8-10]. Le proprietà salutari della cipolla sono spesso attribuite agli alti livelli di due classi di composti nutraceutici: flavonoidi e alk(en)il cisteina solfossidi (ACSO). La prima classe comprende flavonoli e antociani. La quercetina è il principale flavonolo rilevabile, noto per le sue forti proprietà antiossidanti e antinfiammatorie nell'eliminazione dei radicali liberi e nel legame degli ioni dei metalli di transizione ,; mentre gli antociani conferiscono il colore rosso/viola ad alcune varietà di cipolla. Per quanto riguarda gli ACSO, il più abbondante è l'isoalliina [(+)-trans-S-1-propenil-L-cisteina solfossido] ,, un amminoacido solforato non volatile e non proteico immagazzinato nelle cellule, indirettamente responsabile dell'aroma e del gusto pungente delle cipolle ,. Dopo la rottura del tessuto, l'isoalliina viene scissa dall'enzima alliinasi per produrre una serie di composti volatili (piruvato, ammoniaca, tiosolfonati e propanetiale S-ossido) che inducono lacrimazione e causano odore sgradevole (pungenza). ,. Il piccante della cipolla viene spesso misurato come la quantità, per grammo di peso fresco, di acido piruvico generato dall'idrolisi [15.16].
Nei paesi del bacino del Mediterraneo, proposto come uno dei centri di diversità secondaria A. cepa [17.18], i bulbi di cipolla mostrano un'ampia variabilità in forma, dimensione, colore, sostanza secca e piccante [19-uno]. Inoltre, la concimazione a base di zolfo, le pratiche agronomiche, la tipologia del terreno, le condizioni climatiche e il genotipo di cultivar o autoctoni possono influenzare la qualità del bulbo conferendo peculiari valori organolettici e nutrizionali [23-uno]. In Italia, nonostante l’ampia disponibilità di germoplasma della cipolla, solo poche varietà di cipolla sono spesso sottoposte a studi scientifici e adeguatamente caratterizzate [28.29].
Una caratterizzazione genetica e fenotipica approfondita dell’agro-biodiversità è fondamentale per garantire un’adeguata conservazione delle risorse fitogenetiche e promuovere l’uso di genotipi specifici nella catena del valore [30-uno]. I marcatori di ripetizione di sequenza semplice (SSR) sono stati spesso scelti per la mappatura [33-uno], Impronta digitale del DNA e discriminazione delle cultivar [36-uno]e stima affidabile della variabilità genetica all'interno e tra le varietà autoctone [39-uno], poiché sono locus specifici, multiallelici, ereditati in modo codominante, altamente riproducibili e adatti alla genotipizzazione automatizzata.
Nel presente studio, abbiamo focalizzato la nostra attenzione su una varietà autoctona tradizionale pugliese, la “cipolla rossa di Acquaviva” (ARO), coltivata secondo i metodi dell’agricoltura biologica in una piccola area del comune di Acquaviva delle Fonti, in provincia di Bari. (Puglia, Sud Italia). I bulbi di questa varietà autoctona sono grandi, appiattiti e di colore rosso e sono largamente utilizzati nelle ricette locali. Sebbene l’ARO abbia ottenuto il marchio di qualità “Presidio Slow Food”, la sua produzione potrebbe essere ulteriormente promossa e tutelata da marchi di qualità dell’Unione Europea come l’Indicazione Geografica Protetta (IGP) e la Denominazione di Origine Protetta (DOP), poiché questi potrebbero contribuire a limitare la diffusione frodi commerciali e migliorare il reddito dei piccoli proprietari terrieri. In questo studio, i marcatori molecolari SSR sono stati utilizzati come potenti strumenti per valutare la variazione genetica tra le popolazioni ARO e per discriminare questa varietà autoctona da altre due varietà autoctone di cipolla rossa dell’Italia meridionale. Inoltre, abbiamo stimato il piccante e il contenuto di solidi solubili per valutare il sapore ARO in relazione alla domanda del mercato.
Risultati
Istituzione della Raccolta del Germoplasma della Cipolla Rossa Acquaviva e Caratterizzazione Morfologica
I semi di 13 popolazioni autoctone dell'ARO, donati dagli agricoltori nell'ambito del progetto BiodiverSO della Regione Puglia, sono stati utilizzati per costituire una collezione di germoplasma dell'ARO.
I descrittori morfologici, relativi al bulbo, alla buccia e alla polpa, sono stati raccolti sul germoplasma ARO e su tre varietà locali di cipolla, due appartenenti alla varietà locale “Cipolla rossa di Tropea” (TRO) e una alla varietà locale “Cipolla ramata di Montoro” (MCO) (Figura 1). Tutti i bulbi ARO erano piatti ed erano caratterizzati da buccia esterna rossa e polpa con diverse tonalità di rosso. Al contrario, la polpa dei bulbi TRO era completamente rossa, mentre la polpa dei bulbi MCO era scarsamente pigmentata (Tabella S1). L'analisi biochimica ha permesso di valutare il contenuto di solidi solubili e il piccante. Come riportato nella Tav 1, i valori medi del contenuto solido solubile dei bulbi nelle popolazioni ARO erano 7.60 e variavano da 6.00 (ARO12) a 9.50° Brix (ARO11 e ARO13). Questo valore era superiore a quello stimato per le varietà autoctone TRO e MCO (4.25 e 6.00° Brix, rispettivamente).

Tabella 1. Contenuto solido solubile e valori di piccantezza valutati nelle popolazioni di “Cipolla Rossa di Acquaviva” (ARO), “Cipolla Rossa di Tropea” (TRO) e “Cipolla Rame di Montoro” (MCO) *.
| CODICE | Contenuto solido solubile (Brix) | Piccantezza (pmolg-1 stagione) | ||
| Significare | CV y (%) | Significare | CV y (%) | |
| ARO1 | 6.25 D* | 5.65 | 5.84ab* | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 l' | 22.98 |
| ARO3 | 7.50 BCD | 9.42 | 5.28 ab | 22.88 |
| ARO4 | 7.50 BCD | 0.00 | 6.97 l' | 3.74 |
| ARO 5 | 7.50 BCD | 0.00 | 6.80 l' | 9.68 |
| ARO6 | 6.25 D | 5.65 | 4.51 ab | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25 ab | 15.44 |
| ARO8 | 9.00 AB | 0.00 | 7.04 l' | 3.49 |
| ARO9 | 8.25 ABC | 4.28 | 6.84 l' | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94 ab | 6.57 |
| ARO11 | Il 9.50 | 7.44 | 5.54 ab | 16.43 |
| ARO12 | 6.00 D | 0.00 | 4.91 ab | 9.70 |
| ARO13 | Il 9.50 | 7.44 | 6.63 l' | 24.93 |
| MCO | 6.00 D | 0.00 | 4.18 ab | 2.66 |
| TRO1 | 4.25 E | 8.31 | 2.80 b | 2.10 |
| TRO2 | 4.25 E | 8.31 | 4.28 ab | 4.79 |
*Le medie con le stesse lettere maiuscole o minuscole non sono statisticamente diverse rispettivamente a 0.01P o 0.05P (test SNK). y Coefficiente di variazione.
Il valore medio della pungenza ARO, valutato mediante il contenuto di acido piruvico, era 6.00, compreso tra 4.51 pmol g-1 Da FW (ARO6) a 7.04 (ARO8). Questo valore era superiore a quello stimato nelle varietà locali TRO e MCO (3.54 pmol g-1 FW e 4.18 pmol g-1 FW, rispettivamente).
Polimorfismo SSR e relazioni genetiche tra le accessioni
Nel presente studio, 11 delle 37 combinazioni di primer SSR testate hanno fornito polimorfismi a locus singolo, ovvero hanno prodotto al massimo due prodotti di amplificazione in un singolo individuo. Complessivamente, sono stati rilevati 55 alleli in 320 individui con un numero di alleli per locus compreso tra 2 (ACM147 e ACM 504) e 11 (ACM132) e un valore medio di 5 alleli (Tabella 2). Nelle singole popolazioni, il numero di alleli (Na) variava da 1.94 (ACM147 e ACM504) a 5.38 (ACM132), mentre il numero effettivo di alleli (Ne) variava da 1.41 (ACM152) a 2.82 (ACM449). Discrepanze tra i valori di Na e Ne erano dovuti alla presenza di alleli con bassa frequenza nelle popolazioni e alla predominanza di solo pochi alleli. Il valore di eterozigosi (Ho) più alto osservato è stato evidenziato per ACM138 e ACM449 (0.62), mentre quello più basso è stato associato ad ACM152 (0.25). L'eterozigosità prevista (He), che corrisponde all'aspettativa teorica in una popolazione panmittica, variava da 0.37 (ACM504) a 0.61 (ACM132, ACM138 e ACM449). L'indice di fissazione di Wright (Fis), ha mostrato valori prossimi allo zero (media 0.05) per tutti i marcatori, indicando valori simili tra i livelli di eterozigosi osservati e attesi, come previsto per una specie di outcrossing. L'efficienza del singolo marcatore SSR nell'impronta genetica è stata stimata dall'indice del contenuto di informazioni polimorfiche (PIC), con un valore medio di 0.48 e variava da 0.33 (ACM504) a 0.67 (ACM132). Un altro indice di efficienza, lo Shannon's Information Index (I), mostrava un valore medio di 0.84 e i valori presunti variavano da 0.45 (ACM152) a 1.20 (ACM132).
Tabella 2. Caratteristiche del polimorfismo degli 11 marcatori SSR utilizzati per stimare la diversità genetica nelle popolazioni ARO, TRO e MCO. Numero totale di alleli (Na), intervallo di dimensioni della banda e indice del contenuto di informazioni polimorfiche (PIC) Fare riferimento al set totale di 320 individui genotipizzati in questo studio. Numero di alleli (Na), numero di alleli effettivi (Ne), eterozigosità osservata (Ho), eterozigosità attesa (He), indice di fissazione (Fis) e l'Indice di informazione di Shannon (I) si riferiscono a valori medi calcolati da 16 popolazioni, ciascuna composta da 20 individui.
| Luogo. | N. totale | Intervallo di dimensioni (bp) | PIC | Significare | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | all'0.02 ottobre |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | all'0.01 ottobre |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | all'0.06 ottobre |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | all'0.03 ottobre |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| Significare | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
Tra le popolazioni, ARO3, ARO6, ARO8, ARO10, TRO1 e MCO hanno mostrato un alto livello di variazione genetica (Ho > 0.5), mentre la diversità più bassa è stata osservata nella popolazione ARO7 (Ho = 0.27) (Tabella Supplementare S2). Complessivamente tutte le adesioni hanno evidenziato Fis valori prossimi allo zero (Fis valore medio = 0.054), come previsto in condizioni di accoppiamento casuale.
Analisi della varianza molecolare e della struttura genetica
La ripartizione gerarchica della variazione genetica tra e all'interno delle popolazioni è stata calcolata da AMOVA. I risultati hanno evidenziato una frazione considerevole di variazione genetica all’interno delle popolazioni (87%). La variazione tra le popolazioni, 13%, è stata altamente significativa (P < 0.001) (Tabella 3). I valori a coppie del parametro Fpt, un analogo dell'indice di fissazione Fst di Wright, che vanno da 0.002 (ARO2/ARO10) a 0.468 (ARO7/TRO2), erano significativi (P <0.05), ad eccezione di nove confronti a coppie (Tabella Supplementare S3).
Tabella 3. Analisi della varianza molecolare di 320 genotipi di 16 popolazioni di Allium cepa L.
| Fonte | df | Somma dei quadrati | Stima della varianza | Varianza (%) | Fpt | P |
| Tra le popolazioni | 15 | 458.63 | 1.16 | 13% | ||
| All'interno delle popolazioni | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| Totale | 319 | 2731.62 | 8.66 |
Indagine sulla struttura genetica nel A. cepa la raccolta genotipizzata in questo studio è stata eseguita mediante l'analisi di clustering basata su modelli di mescolanza implementata nel software STRUCTURE. Il metodo Evanno AK ha suggerito la suddivisione in due cluster (K = 2) come quella più informativa per il nostro dataset,con the GENERAZIONE pe più altoak a K = 5 (Figura complementare S1). UN forchetta = 2, aCVopulazioni wqui culoigned purenef i due cluster con un coefficiente di rnernbertoip (q) > 0.7. Come shoentrare figura 2a, il primo cluster (denominato S1) includeva MCO e tutte le popolazioni ARO, mentre il cluster S2 raggruppava le due popolazioni TRO. A K = 5, fornendo una descrizione più approfondita del set di dati (Figura 2b), il 75% delle adesioni sono state assegnate a uno dei cinque cluster. La separazione tra ARO (S1) e TRO (S2) è stata confermata, sebbene alcune popolazioni ARO siano state mescolate (q <0.7) o raggruppate separatamente nei due nuovi cluster S3 e S4 (ARO7 e ARO12, rispettivamente). È interessante notare che la tipologia commerciale MCO formava un cluster distinto (S5) separato dalla cipolla rossa pugliese.
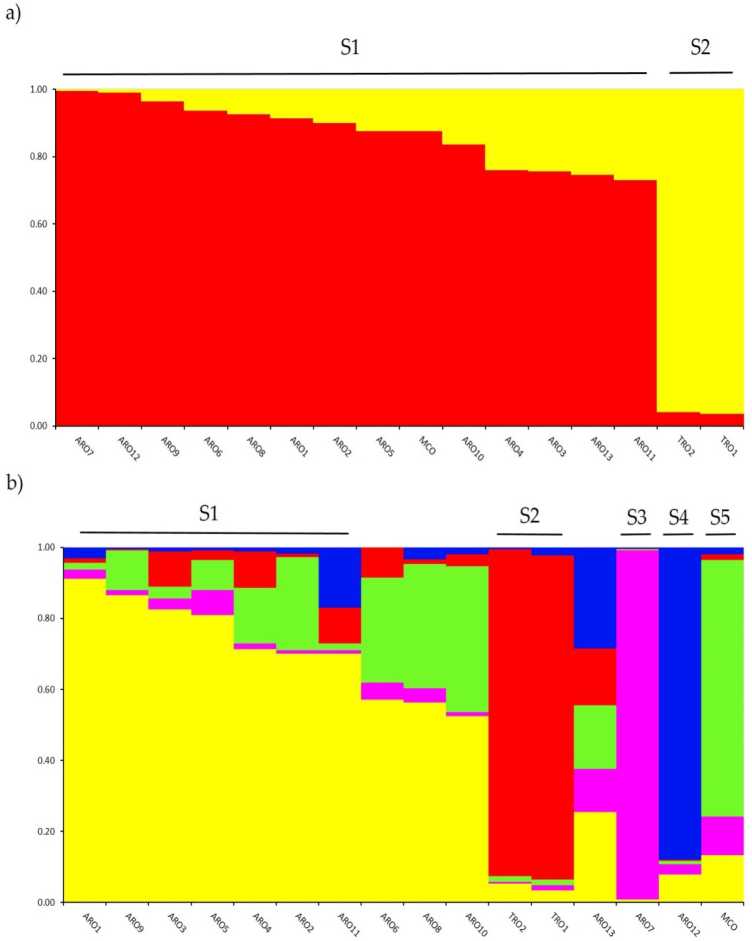
Relazioni genetiche tra le popolazioni
Il polimorfismo SSR ha permesso di tracciare un dendrogramma della diversità genetica e i risultati dell'analisi filogenetica sono mostrati in Figura 3a. Qui, la raccolta di germoplasma è stata suddivisa in cinque gruppi fortemente supportati da valori bootstrap. Le popolazioni ARO7 e ARO12 sono state immediatamente separate dalle restanti popolazioni e hanno formato due cluster distinti. Il terzo cluster comprendeva le due popolazioni commerciali di TRO, mentre il quarto nodo divideva MCO da undici popolazioni ARO. La relazione genetica che si verifica tra le popolazioni è stata ulteriormente studiata mediante l'analisi delle coordinate principali (PCoA) (Figura 3b). Come evidenziato in precedenza, le popolazioni ARO erano raggruppate strettamente, ad eccezione di ARO12 e ARO7, che apparivano in posizioni isolate nel grafico PCoA. Le due popolazioni TRO e MCO erano sparse nel pannello in basso a destra del grafico.
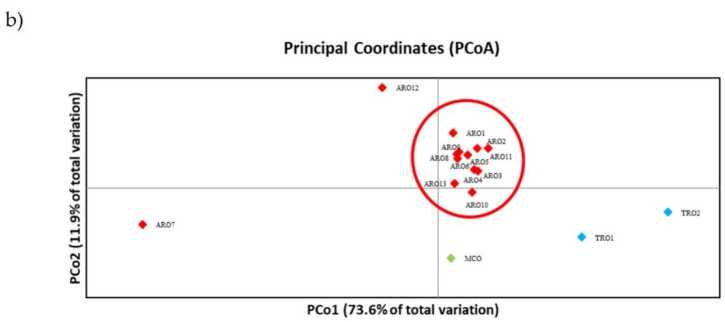
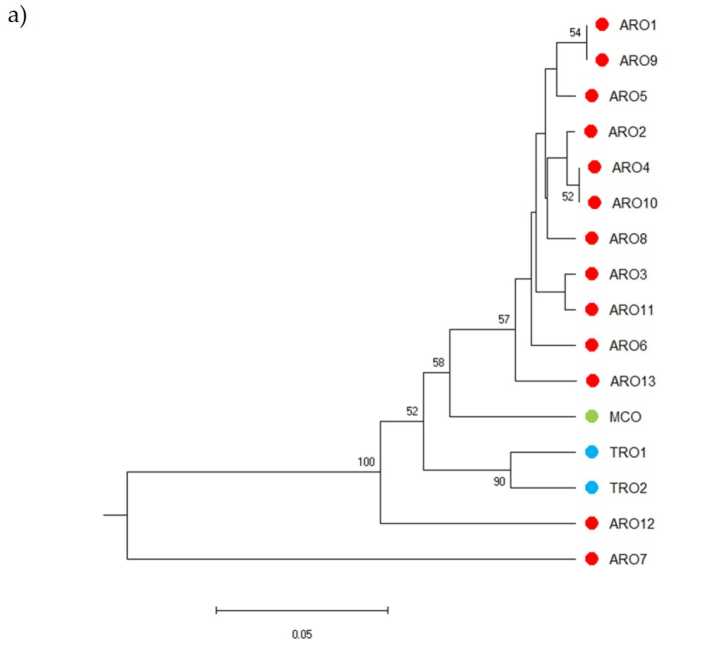
Immagine 3. Diversità genetica tra 16 A. cepa popolazioni caratterizzate in questo studio, in base al loro profilo SSR. (a) Dendrogramma UPGMA della distanza genetica. I valori di supporto Bootstrap >50 sono indicati sopra i nodi corrispondenti; (b) analisi delle componenti principali (PCoA). Il cluster cerchiato in rosso corrisponde perfettamente al gruppo generato dall'analisi filogenetica e costituito da 11 accessioni ARO.
Discussione
All’interno della grande quantità di agro-biodiversità tradizionalmente coltivata nel Sud Italia, le varietà autoctone di cipolla rappresentano prodotti di nicchia che devono essere preservati dal rischio di erosione genetica e dalla minaccia di sostituzione con cultivar moderne. Nell'ambito del progetto regionale BiodiverSO, volto a raccogliere, caratterizzare, promuovere e salvaguardare le risorse genetiche della regione Puglia fortemente legate al patrimonio locale, abbiamo costituito una raccolta di semi di 13 popolazioni della varietà autoctona ARO. Abbiamo riportato la prima valutazione della variazione dell'ARO in termini di polimorfismi del DNA e di due parametri biochimici, contenuto di solidi solubili e acido piruvico, correlati ai tratti aromatici e importanti per l'accettazione dei prodotti freschi non cotti. Inoltre, i dati sulla varietà autoctona ARO sono stati confrontati con quelli raccolti su altre due varietà autoctone di cipolla pigmentata con le quali veniva spesso confusa.
Le analisi biochimiche hanno evidenziato la dolcezza delle 13 popolazioni ARO, correlata all'elevato contenuto di solidi solubili e al piccante medio, secondo le linee guida dell'industria della cipolla dolce ,. I bulbi ARO erano più dolci di quelli delle varietà autoctone TRO e MCO e mostravano un sapore piccante leggermente superiore. Tuttavia, la dolcezza delle cipolle è dovuta ad un equilibrio tra contenuto di zucchero e piccantezza, pertanto questa caratterizzazione potrebbe essere utile per supportare la selezione di genotipi di pregio, solitamente effettuata dagli agricoltori solo in base alla morfologia.
I marcatori SSR si sono confermati uno strumento utile per discriminare i genotipi, sebbene raccolti all'interno di un'area ristretta come il comune di Acquaviva delle Fonti. I marcatori selezionati mostravano un numero maggiore di alleli rispetto ai marcatori precedentemente riportati da , ed ,, ma inferiore ai marcatori riportati da ,. Inoltre, il 50% del nostro set di marcatori ha mostrato valori di indice PIC superiori a 0.5, rivelandosi idonei a discriminare le popolazioni della raccolta, come suggerito da ,. La valutazione della diversità all'interno delle popolazioni ha rivelato valori simili tra Ho e He, con conseguente basso Fis valori. Ciò è in accordo con la natura di incrocio di A. cepa, che soffre gravemente di depressione da consanguineità ,. La Fi complessivas Il valore calcolato nelle popolazioni di cipolle considerate in questo studio (0.054) era inferiore a quello precedentemente riportato da , (0.22) e quasi identico a quello trovato da , (0.08) e , (0.00) che hanno valutato la diversità genetica nelle varietà autoctone di cipolle rispettivamente della Spagna nordoccidentale e del Niger. Livelli notevoli di eterozigosi nelle popolazioni ARO rafforzano l’idea che la Puglia rappresenta un centro di diversità per molte specie orticole [32, 42, 49-uno].
L'AMOVA ha evidenziato che la maggior parte delle variazioni molecolari nella raccolta genotipizzata in questo studio si trova all'interno delle popolazioni. Tuttavia, una significativa differenziazione genetica tra le popolazioni (FPT valori) hanno rivelato la presenza di stratificazione genetica. Infatti, sebbene i nostri risultati indicassero la presenza di uniformità genetica nella maggior parte delle popolazioni ARO, formando un cluster ben definito, le popolazioni ARO7 e ARO12 mostravano un profilo genetico chiaramente distinto. Questo risultato potrebbe essere dovuto ad una diversa origine dei semi utilizzati dai due agricoltori da cui sono state raccolte le popolazioni. Inoltre, sulla base dei risultati ottenuti, la varietà autoctona ARO può essere considerata chiaramente distinta a livello genetico dalle varietà autoctone TRO e MCO. In uno studio recente, , ha valutato la diversità genetica di diverse varietà autoctone di cipolla italiane, tra cui “Acquaviva”, “Tropea” e “Montoro”. Sebbene gli autori abbiano utilizzato marcatori SNP per valutare la diversità genetica di una collezione più ampia di cipolle, la genotipizzazione non è stata in grado di discriminare “Acquaviva” dalle cipolle “Tropea” e “Montoro”. Probabilmente, questa discrepanza è dovuta al basso valore medio del PIC riscontrato (0.292), suggerendo una modesta informatività generale dei loci in analisi come sostenuto da ,. Inoltre, per indagare la presenza di sottostrutture nel loro cluster italiano, sarebbe stato meglio analizzare i genotipi italiani separatamente dal resto della collezione. Probabilmente avrebbe permesso di visualizzare modelli di diversità genetica legati alla stratificazione geografica o a tratti sottoposti a selezione empirica.
In conclusione, il presente studio rappresenta un rapporto completo su una varietà autoctona di cipolla associata al patrimonio culturale locale e di importanza economica per gli agricoltori. I nostri risultati evidenziano che, con poche eccezioni, ARO è caratterizzato da un pool genetico ben definito, che merita di essere preservato dal rischio di erosione genetica. Pertanto, la creazione di una collezione rappresentativa di questa preziosa fonte di diversità genetica è stata cruciale. Infine, la caratterizzazione genetica e fenotipica degli ARO potrebbe essere utile per ottenere marchi di qualità da parte dell'Unione Europea.
Materiali e Metodi
Raccolta del germoplasma, materiale vegetale ed estrazione del DNA
Un insieme di 13 popolazioni della varietà autoctona ARO sono state acquisite nell'ambito di un progetto della Regione Puglia (BiodiverSO: https://www.biodiversitapuglia.it/), attraverso una serie di missioni svolte ad “Acquaviva delle Fonti”, un piccolo comune pugliese in provincia di Bari, Italia. I siti di raccolta di ciascuna accessione sono stati mappati attraverso il Sistema Informativo Geografico (GIS) e riportati in Tabella 4. Inoltre, nel presente studio sono state incluse e utilizzate come riferimenti due popolazioni della varietà autoctona TRO e una popolazione della razza autoctona MCO. Tutto il materiale vegetale è stato coltivato nelle stesse condizioni ambientali presso l'azienda sperimentale “P Martucci” dell'Università di Bari (41° 1'22.08″ N, 16°54'25.95″ E), sotto gabbia di protezione per evitare l'impollinazione incrociata tra popolazioni e garantendo l’impollinazione intra-popolazione mediante mosconi (Lucilia Cesare). Le 16 popolazioni sono state caratterizzate per tratti legati alla dimensione e alla forma del bulbo e al colore della pelle e della polpa (Tabella S1). Inoltre, è stata eseguita l'analisi del contenuto solido solubile utilizzando un rifrattometro portatile ed è stata misurata la piccantezza nei campioni di succo di cipolla aggiungendo 2,4-dinitrofenil idrazina (0.125% v/v in 2N di HCl) e valutando l'assorbanza a 420 nm, come riportato da ,. Sono stati effettuati il test a range multiplo di Duncan e il test SNK per determinare la presenza di differenze significative.
Tabella 4. Elenco delle popolazioni raccolte e genotipizzate in questo studio. Per ciascuna popolazione vengono riportati il codice identificativo, il nome locale, le coordinate GPS e la banca genetica che preserva i semi.
| Code | Nome | Coordinate GPS | Banca genetica y |
| ARO1 | Cipolla rossa di Acquaviva | 40°54’21.708″ N 16°49’1.631” E | Di.SSPA |
| ARO2 | Cipolla rossa di Acquaviva | 40°53’14.28″ N 16°48’56.879” E | Di.SSPA |
| ARO3 | Cipolla rossa di Acquaviva | 40°54’11.304″ N 16°49’13.079” E | Di.SSPA |
| ARO4 | Cipolla rossa di Acquaviva | 40°54’3.348″ N 16°40’27.011” E | Di.SSPA |
| ARO5 | Cipolla rossa di Acquaviva | 40°51’59.76″ N 16°53’0.527” E | Di.SSPA |
| ARO6 | Cipolla rossa di Acquaviva | 40°52’48.72″ N 16°49’43.247” E | Di.SSPA |
| ARO7 | Cipolla rossa di Acquaviva | 40°53’13.47″ N 16°50’23.783” E | Di.SSPA |
| ARO8 | Cipolla rossa di Acquaviva | 40°53’18.816″ N 16°49’33.888” E | Di.SSPA |
| ARO9 | Cipolla rossa di Acquaviva | 40°54'51.372″N16°49'3.504" E | Di.SSPA |
| ARO10 | Cipolla rossa di Acquaviva | 40°54’1.188″ N 16°49’24.311” E | Di.SSPA |
| ARO11 | Cipolla rossa di Acquaviva | 40°52'49.8″N16°49'48.575" E | Di.SSPA |
| ARO12 | Cipolla rossa di Acquaviva | 40°52’38.892″ N 16°49’28.379” E | Di.SSPA |
| ARO13 | Cipolla rossa di Acquaviva | 40°53’21.768″ N 16°49’29.711” E | Di.SSPA |
| TRO1 | Cipolla rossa lunga di Tropea | - | Di.SSPA |
| TRO2 | Cipolla rossa tonda di Tropea | - | Di.SSPA |
| MCO | Cipolla ramata di Montoro | - | Di.SSPA |
| y Di.SSPA, Dipartimento di Scienze del Suolo, della Pianta e degli Alimenti, Università degli Studi di Bari. |
Materiale fogliare di 20 genotipi per popolazione è stato campionato e conservato a -80 °C fino all'uso. Per le specie ricche di polisaccaridi, come A. cepa, i primi passaggi per rimuovere il polisaccaride sono essenziali per ottenere DNA di buona qualità, pertanto i lavaggi iniziali in tampone STE (saccarosio 0.25 M, Tris 0.03 M, EDTA 0.05 M) sono stati eseguiti come descritto da ,. Il DNA totale è stato estratto seguendo il metodo CTAB , e infine è stato controllato la qualità e la concentrazione mediante lo spettrofotometro UV-vis Nano Drop 2000 (ThermoScientific, Waltham, MA, USA) e l'elettroforesi su gel di agarosio allo 0.8%.
Analisi SSR
16 combinazioni di primer EST-SSR sviluppate da , e precedentemente testato in studi sulla diversità genetica da , ed , e 21 SSR genomici [45-uno] sono stati selezionati per valutarne l'idoneità (Tabella Supplementare S4). La genotipizzazione è stata eseguita utilizzando il metodo economico di etichettatura fluorescente in cui la coda M13 viene aggiunta a ciascun primer SSR diretto ,. Le miscele PCR sono state preparate in una reazione da 20 gL contenente: 50 ng di DNA totale, 0.2 mM di miscela dNTP, 1X di tampone di reazione PCR, 0.8 U di DreamTaq DNA polimerasi (Thermo Scientific, Waltham, MA, USA), 0.16 gM di primer inverso , 0.032 gM di primer forward esteso con la sequenza M13 (5′-TGTAAAACGACGGCCAGT-3 ′) e 0.08 gM di un primer M13 universale etichettato con coloranti fluorescenti FAM o NED (Sigma-Aldrich, St. Louis, MO, USA). Le reazioni PCR sono state condotte nel termociclatore SimpliAmp (Applied Biosystems, CA, USA) con le seguenti condizioni per la maggior parte delle coppie di primer: 94 °C per 5 minuti, 40 cicli a 94 °C per 30 s, 58 °C per 45 s e 72 °C per 45 s e un allungamento finale a 72 °C per 5 min. Per quanto riguarda ACM446 e ACM449, è stata applicata una PCR touchdown con ricottura da 60 °C a 55 °C su 10 cicli, 30 cicli a 55 °C, seguita da un'estensione finale di 5 minuti a 72 °C. I prodotti PCR sono stati caricati in una piastra da 96 pozzetti e miscelati con 14 gL di Hi-Di Formamide (Life Technologies, Carlsbad, CA, USA) e 0.5 gL di GeneScan 500 ROX Size Standard (Life Technologies, Carlsbad, CA, USA). Gli ampliconi sono stati risolti mediante la macchina per sequenziamento capillare ABI PRISM 3100 Avant Genetic Analyser (Life Technologies, Carlsbad, CA, USA), dove gli alleli sono stati valutati come codominanti e assegnati utilizzando il software GeneMapper versione 3.7.
I software GenAlEx 6.5 , e Cervus 3.0.7 , sono stati utilizzati per stimare il numero di alleli (Na), il numero di alleli effettivi (Ne), l'eterozigosi osservata (Ho), l'eterozigosi attesa (He), il contenuto informativo polimorfico (PIC), l'indice informativo di Shannon (I) e l'indice di fissazione (Fis ) per ciascun locus SSR.
Valutazione della diversità genetica
La partizione gerarchica della variazione genetica tra e all'interno delle popolazioni di cipolle è stata valutata da GenAlEx 6.5 , attraverso l'analisi della varianza molecolare (AMOVA) con bootstrap 999 per testarne la significatività. Inoltre, il software GenAlEx 6.5 è stato utilizzato per stimare la diversità all'interno di ciascuna popolazione calcolando la media di Ho, He e Fis su tutti i loci SSR.
La struttura della popolazione è stata dedotta dall'algoritmo di clustering basato sul modello bayesiano implementato nel software STRUCTURE v.2.3.4 ,. Il set di dati è stato eseguito con un numero di ipotetici cluster (K), compresi tra 1 e 10, impostando dieci esecuzioni indipendenti per ciascun valore K. Per ciascuna analisi, con l'obiettivo di verificare la coerenza dei risultati, sono stati eseguiti 100,000 periodi di burn-in iniziale e 100,000 iterazioni della catena Markov Monte Carlo (MCMC) con il modello di mescolanza e frequenze alleliche indipendenti tra le popolazioni. Il valore K più probabile è stato determinato implementando il metodo AK, descritto da ,, nel programma basato sul web STRUCTURE HARVESTER ,. Una singola popolazione veniva assegnata a un cluster specifico quando il suo coefficiente di appartenenza (valore q) era superiore a 0.7, altrimenti era considerata di discendenza mista.
L'analisi delle coordinate principali è stata eseguita al fine di visualizzare modelli di relazione genetica tra le accessioni rivelate dalla matrice della distanza genetica di Nei (Tabella Supplementare S5). Sulla base delle frequenze alleliche, è stato costruito un dendrogramma della distanza genetica implementando il metodo dei gruppi di coppie non ponderate con medie aritmetiche (UPGMA) analisi dei cluster nel software POPTREEW ,. È stato applicato il bootstrap per valutare la fiducia nel clustering gerarchico, impostando 100 ricampionamenti del set di dati. Infine, il software MEGA X , è stato utilizzato come software per il disegno degli alberi.
Materiali supplementari: Di seguito sono disponibili online all'indirizzo http://www.mdpi.com/2223-7747/9/2/260/s1. Tabella S1: Caratterizzazione morfologica dei bulbi ARO, MCO e TRO. Tabella S2: Indici di eterozigosità e fissazione calcolati per varietà locali ARO e varietà locali TRO e MCO. Tabella S3: Valori a coppie del parametro Fpt. Tabella S4: Elenco degli SSR utilizzati nello studio. Tabella S5. Matrice di popolazione a coppie della distanza genetica Nei. Figura S1: grafico a linee dei valori K che cambiano con il Delta K di Evanno.
Contributi degli autori: CL e LR hanno concepito lo studio e progettato l'esperimento; CL e PI hanno eseguito l'analisi dei marcatori molecolari; ARM e VZ hanno eseguito le prove sul campo; RM, SP, GR e CL sono stati coinvolti nell'analisi dei dati; RM e CL hanno scritto il manoscritto. Tutti gli autori hanno letto e accettato la versione pubblicata del manoscritto.
finanziamento: Questo lavoro è stato finanziato dal progetto Regionale Puglia “Biodiversità delle specie vegetali pugliesi”—Programma di Sviluppo Rurale per la Puglia 2014-2020. Misura 10—Sottomisura 10.2; borsa di studio CUP H92C15000270002, Italia.
Ringraziamenti: Si ringraziano l’“Azienda Agricola Iannone Anna” e l’”Associazione produttori della vera cipolla rossa di Acquaviva” per aver fornito il materiale vegetale utilizzato nell’esperimento.
Conflitti di interesse: Gli autori dichiarano assenza di conflitto di interesse.
Riferimenti
- 1. Stearn, WT Quante specie di Allium sono conosciute? KewMag. 1992, 9, 180-182. [CrossRef]
- 2. FAOSTAT. Database statistico della FAO. Disponibile online: http://www.fao.org/2017 (accesso effettuato l'8 gennaio 2019).
- 3. Block, E. La chimica dell'aglio e della cipolla. Sci. Am. 1985, 252, 114-119. [CrossRef]
- 4. Lee, B.; Jung, JH; Kim, HS Valutazione della cipolla rossa sull'attività antiossidante nel ratto. Chimica alimentare. Tossico. 2012, 50, 3912-3919. [CrossRef]
- 5. Lee, SM; Luna, J.; Chung, JH; Cha, YJ; Shin, MJ Effetto degli estratti di buccia di cipolla ricchi di quercetina sulla trombosi arteriosa nei ratti. Chimica alimentare. Tossico. 2013, 57, 99-105. [CrossRef] [PubMed]
- 6. Yoshinari, O.; Shiojima, Y.; Igarashi, K. Effetti anti-obesità dell'estratto di cipolla nei ratti grassi diabetici zucker. Nutrienti 2012, 4,1518-1526. [CrossRef]
- 7. Akash, MSH; Rehman, K.; Chen, S. Pianta delle spezie Allium cepa: integratore alimentare per il trattamento del diabete mellito di tipo 2. Alimentazione 2014, 30, 1128-1137. [CrossRef] [PubMed]
- 8. Wang, Y.; Tian, WX; Ma, XF Effetti inibitori della cipolla (Allium cepa L.) estratto sulla proliferazione delle cellule tumorali e degli adipociti attraverso l'inibizione della sintasi degli acidi grassi. Pac asiatico. J. Cancro Prec. 2012,13, 5573-5579. [CrossRef] [PubMed]
- 9. Lai, WW; Hsu, Carolina del Sud; Chueh, FS; Chen, YY; Yang, JS; Lin, JP; Vincolo, JC; Tsai, CH; Chung, JG La quercetina inibisce la migrazione e l'invasione delle cellule di cancro orale umano SAS attraverso l'inibizione delle vie di segnalazione di NF-kappaB e della metalloproteinasi della matrice-2/-9. Anticancro Res. 2013, 33, 1941-1950. [PubMed]
- 10. Nicastro, HL; Ross, SA; Milner, JA Aglio e cipolle: le loro proprietà di prevenzione del cancro. Cancro Prec. ris. 2015, 8,181-189. [CrossRef]
- 11. Forte, L.; Torricelli, P.; Boanini, E.; Gazzano, M.; Rubini, K.; Fini, M.; Bigi, A. Proprietà antiossidanti e di riparazione ossea dell'idrossiapatite funzionalizzata con quercetina: uno studio di co-coltura di cellule osteoblasti-osteoclasti-endoteliali in vitro. Acta Biomater. 2016, 32, 298-308. [CrossRef]
- 12. Yamazaki, Y.; Iwasaki, K.; Mikami, M.; Yagihashi, A. Distribuzione di undici precursori aromatici, derivati S-Alk (en) il-L-cisteina, in sette verdure Allium. Scienza dell'alimentazione Tecnologia. Ris. 2011, 17, 55-62. [CrossRef]
- 13. Block, E. La chimica dell'organozolfo del genere Allium: implicazioni per la chimica organica dello zolfo. Angelo. chimica Int. Ed. inglese 1992, 31, 1135-1178. [CrossRef]
- 14. Griffiths, G.; Trueman, L.; Crowther, T.; Tommaso, B.; Smith, B. Onions: un vantaggio globale per la salute. Fitother. ris. 2002,16, 603-615. [CrossRef]
- 15. Schwimmer, S.; Weston, WJ Sviluppo enzimatico dell'acido piruvico nella cipolla come misura della piccantezza. J. Agric. chimica alimentare. 1961, 9, 301-304. [CrossRef]
- 16. Ketter, GATTO; Randle, WM Valutazione della piccantezza delle cipolle. In Studi testati per l'insegnamento di laboratorio; Karcher, SJ, ed.; Associazione per la formazione nei laboratori di biologia (ABLE): New York, NY, USA, 1998; Volume 19, pp. 177-196.
- 17. Hanelt, P Tassonomia, evoluzione e storia. In Cipolle e colture affini, vol. I. Botanica, Fisiologia e Genetica; Rabinowitch, HD, Brewster, JL, a cura di; CRC Press: Boca Raton, Florida, Stati Uniti, 1990; pp. 1-26.
- 18. Rabinostrega, HD; Curra, L. Scienza delle colture di allium: progressi recenti; CABI Publishing: Wallingford, Regno Unito, 2002.
- 19. Mallor, C.; Carravedo, M.; Estopanan, G.; Mallor, F. Caratterizzazione delle risorse genetiche della cipolla (Allium cepa L.) dal centro secondario della diversità spagnolo. Durata. J. Agric. Ris. 2011, 9, 144-155. [CrossRef]
- 20. Ferioli, F.; D'Antuono, LF Valutazione dei composti fenolici e dei solfossidi di cisteina nel germoplasma locale di cipolla e scalogno provenienti da Italia e Ucraina. Genetta. Risorsa. Ritaglia Evol. 2016, 63, 601-614. [CrossRef]
- 21. Petropoulos, SA; Fernandes, A.; Barros, L.; Ferreira, ICFR; Ntatsi, G. Descrizione morfologica, nutrizionale e chimica del "vatikiotiko", una varietà locale di cipolla proveniente dalla Grecia. chimica alimentare. 2015,182, 156-163. [CrossRef]
- 22. Liguori, L.; Adiletta, G.; Nazzaro, F.; Fratianni, F.; Di Matteo, M.; Albanese, D. Proprietà biochimiche, antiossidanti e attività antimicrobica di diverse varietà di cipolla nell'area mediterranea. J. Misurazioni alimentari. Carattere. 2019,13, 1232-1241. [CrossRef]
- 23. Ehi, KS; Luccio, L.; Crosby, K.; Jones, R.; Leskovar, D. Differenze nella piccantezza della cipolla dovute a cultivar, ambiente di crescita e dimensioni del bulbo. Sci. Ortico. 2006,110, 144-149. [CrossRef]
- 24. Beesk, N.; Perner, H.; Schwarz, D.; Giorgio, E.; Kroh, LW; Rohn, S. Distribuzione di quercetina-3, 4′-O-diglucoside, quercetina-4′-O-monoglucoside e quercetina in diverse parti del bulbo di cipolla (Allium cepa L.) influenzata dal genotipo. chimica alimentare. 2010,122, 566-571. [CrossRef]
- 25. Caruso, G.; Conti, S.; Villari, G.; Borrelli, C.; Melchionna, G.; Minutolo, M.; Russo, G.; Amalfitano, C. Effetti del tempo di trapianto e della densità delle piante sulla resa, sulla qualità e sul contenuto di antiossidanti della cipolla (Allium cepa L.) nell'Italia meridionale. Sci. Ortico. 2014,166, 111-120. [CrossRef]
- 26. Perez-Gregorio, MR; Regueiro, J.; Simal-Gandara, J.; Rodrigues, AS; Almeida, DPF Aumentare il valore aggiunto delle cipolle come fonte di flavonoidi antiossidanti: una revisione critica. Crit. Rev. Food Sci. Nutr. 2014, 541050-1062. [CrossRef] [PubMed]
- 27. Pohnl, T.; Schweiggert, RM; Carle, R. Impatto del metodo di coltivazione e selezione della cultivar sui carboidrati solubili e sui principi pungenti nelle cipolle (Allium cepa l.). J. Agric. chimica alimentare. 2018, 66, 12827-12835. [CrossRef] [PubMed]
- 28. Tedesco, I.; Carbone, V.; Spagnuolo, C.; Minasi, P.; Russo, GL Identificazione e quantificazione dei flavonoidi di due cultivar dell'Italia meridionale Allium cepa L., Tropea (cipolla rossa) e Montoro (cipolla ramata), e la loro capacità di proteggere gli eritrociti umani dallo stress ossidativo. J. Agric. chimica alimentare. 2015, 63, 5229-5238. [CrossRef]
- 29. Villano, C.; Esposito, S.; Carucci, F.; Frusciante, L.; Carputò, D.; Aversano, R. La genotipizzazione ad alto rendimento nella cipolla rivela la struttura della diversità genetica e SNP informativi utili per l'allevamento molecolare. Mol. Razza. 2019, 39 5. [CrossRef]
- 30. Mercati, F.; Longo, C.; Poma, D.; Araniti, F.; Lupini, A.; Mammano, MM; Fiore, MC; Abenavoli, MR; Sunseri, F Variazione genetica di un pomodoro italiano a lunga conservazione (Solanum lycopersicum L.) raccolta utilizzando SSR e caratteristiche morfologiche del frutto. Genetta. Risorsa. Ritaglia Evol. 2014, 62, 721-732. [CrossRef]
- 31. Gonzalez-Perez, S.; Mallor, C.; Garces-Claver, A.; Merino, F.; Taboada, A.; Rivera, A.; Pomar, F.; Perovic, D.; Silvar, C. Esplorando la diversità genetica e i tratti di qualità in una raccolta di cipolla (Allium cepa L.) varietà autoctone della Spagna nordoccidentale. Genetica 2015, 47, 885-900. [CrossRef]
- 32. Lotti, C.; Iovieno, P.; Centomani, I.; Marcotrigiano, AR; Fanelli, V.; Mimiola, G.; Summo, C.; Pavan, S.; Ricciardi, L. Caratterizzazione genetica, bioagronomica e nutrizionale del cavolo riccio (Brassica oleracea L. var. accettarlo) diversità in Puglia, Italia meridionale. Diversità 2018,10 25. [CrossRef]
- 33. Bardaro, N.; Marcotrigiano, AR; Bracuto, V.; Mazzeo, R.; Ricciardi, F.; Lotti, C.; Pavan, S.; Ricciardi, L. Analisi genetica della resistenza a Orobanche crenata (Forsk.) in un pisello (Pisum sativum L.) linea a basso strigolattone. J. Pianta Pathol. 2016, 98 671-675.
- 34. Wako, T.; Tsukazaki, H.; Yaguchi, S.; Yamashita, K.; Ito, S.; Shigyo, M. Mappatura dei loci dei tratti quantitativi per il tempo di imbullonatura nel raggruppamento della cipolla (Allium fistulosum l.). Eufitica 2016, 209, 537-546. [CrossRef]
- 35. Dacca, N.; Mukhopadhyay, A.; Paritosh, K.; Gupta, V.; Pentale, D.; Pradhan, AK Identificazione di SSR genici e costruzione di una mappa di collegamento basata su SSR in Brassica juncea. Euphytica 2017, 213, 15. [CrossRef]
- 36. Anandhan, S.; Mote, SR; Gopal, J. Valutazione dell'identità varietale della cipolla utilizzando marcatori SSR. Seme Sci. Tecnologia. 2014, 42, 279-285. [CrossRef]
- 37. Mitrova, K.; Svoboda, P.; Ovesna, J. La selezione e la validazione di un set di marcatori per la differenziazione delle cultivar di cipolla dalla Repubblica Ceca. Il ceco J. Genet. Razza vegetale. 2015, 51, 62-67. [CrossRef]
- 38. Di Rienzo, V.; Miazzi, MM; Fanelli, V.; Sabetta, W.; Montemurro, C. La conservazione e la caratterizzazione della biodiversità del germoplasma olivicolo pugliese. Acta Hortic. 2018,11991-6. [CrossRef]
- 39. Mallor, C.; Arnedo-Andrés, A.; Garces-Claver, A. Valutare la diversità genetica dello spagnolo Allium cepa varietà autoctone per la coltivazione della cipolla utilizzando marcatori microsatelliti. Sci. Ortico. 2014,170, 24-31. [CrossRef]
- 40. Rivera, A.; Mallor, C.; Garces-Claver, A.; Garcia-Ulloa, A.; Pomar, F.; Silvar, C. Valutare la diversità genetica nella cipolla (Allium cepa L.) varietà autoctone della Spagna nord-occidentale e confronto con la variabilità europea. NZJ raccolto Hortic. 2016, 44, 103-120. [CrossRef]
- 41. De Giovanni, C.; Pavan, S.; Taranto, F.; Di Rienzo, V.; Miazzi, MM; Marcotrigiano, AR; Mangini, G.; Montemurro, C.; Ricciardi, L.; Lotti, C. Variazione genetica di una raccolta globale di germoplasma di ceci (Cicer arietinum L.) comprese le accessioni italiane a rischio di erosione genetica. Fisiolo. Mol. Biol. Impianti 2017, 23, 197-205. [CrossRef]
- 42. Mazzeo, R.; Morgese, A.; Sonnante, G.; Zuluaga, DL; Pavan, S.; Ricciardi, L.; Lotti, C. Diversità genetica nella rabbia dei broccoli (Brassica rapa L. subsp. silvestris (L.) Janch.) dal Sud Italia. Sci. Ortico. 2019, 253, 140-146. [CrossRef]
- 43. Jakse, M.; Martin, W.; McCallum, J.; Havey, M. Polimorfismi a singolo nucleotide, indel e ripetizioni di sequenze semplici per l'identificazione di cultivar di cipolla. Marmellata. Soc. Ortico. Sci. 2005,130, 912-917. [CrossRef]
- 44. McCallum, J.; Thomson, S.; Pither-Joyce, M.; Kenel, F. Analisi della diversità genetica e sviluppo di marcatori di polimorfismo a singolo nucleotide nella cipolla a bulbo coltivata sulla base di marcatori di ripetizione di sequenza semplice tag-sequenza espressa. Marmellata. Soc. Ortico. Sci. 2008,133, 810-818. [CrossRef]
- 45. Baldovino, S.; Pither-Joyce, M.; Wright, K.; Chen, L.; McCallum, J. Sviluppo di robusti marcatori di ripetizione di sequenze genomiche semplici per la stima della diversità genetica all'interno e tra i bulbi di cipolla (Allium cepa L.) popolazioni. Mol. Razza. 2012, 30, 1401-1411. [CrossRef]
- 46.DeWoody, JA; Honeycutt, RL; Skow, LC Marcatori microsatellitari in cervo dalla coda bianca. J. Hered. 1995, 86 317-319. [CrossRef] [PubMed]
- 47. Khodadadi, M.; Hassanpanah, D. cipolla iraniana (Allium cepa L.) risposte di cultivar alla depressione da consanguineità. Applicazione mondiale Sci. J. 2010,11, 426-428.
- 48. Abdou, R.; Bakasso, Y.; Saadou, M.; Baudoin, JP; Hardy, OJ Diversità genetica delle cipolle del Niger (Allium cepa L.) valutati mediante semplici marcatori di ripetizione di sequenze (SSR). Acta Hortic. 2016,1143 77-90. [CrossRef]
- 49. Pavan, S.; Lotti, C.; Marcotrigiano, AR; Mazzeo, R.; Bardaro, N.; Bracuto, V.; Ricciardi, F.; Taranto, F.; D'Agostino, N.; Schiavulli, A.; et al. Un cluster genetico distinto nei ceci coltivati, come rivelato dalla scoperta di marcatori dell'intero genoma e dalla genotipizzazione. Genoma vegetale 2017, 201710 [CrossRef]
- 50. Pavan, S.; Marcotrigiano, AR; Ciani, E.; Mazzeo, R.; Zonno, V.; Ruggieri, V.; Lotti, C.; Ricciardi, L. Genotipizzazione mediante sequenziamento di un melone (Cucumismelo L.) la raccolta di germoplasma da un centro secondario di diversità evidenzia modelli di variazione genetica e caratteristiche genomiche di diversi pool genetici. Genoma BMC. 2017, 18 59. [CrossRef]
- 51. Di Rienzo, V.; Sion, S.; Taranto, F.; D'Agostino, N.; Montemurro, C.; Fanelli, V.; Sabetta, W.; Boucheffa, S.; Tamendjari, A.; Pasqualone, A.; et al. Flusso genetico tra le popolazioni olivicole del bacino del Mediterraneo. Peer J. 2018, 6. [CrossRef]
- 52. Pastore, LD; McLay, TG Due protocolli su microscala per l'isolamento del DNA da tessuti vegetali ricchi di polisaccaridi. J.Ris.Impianto 2011,124, 311-314. [CrossRef]
- 53. Doyle, JJ; Doyle, JL Isolamento del DNA vegetale da tessuto fresco. Focus 1990,12, 13-14.
- 54. Kuhl, JC; Cheung, F.; Qiaoping, Y.; Martin, W.; Zewdie, Y.; McCallum, J.; Catanach, A.; Rutherford, P.; Lavello, KC; Jenderek, M.; et al. Un set unico di 11,008 tag di sequenza espressa di cipolla rivela la sequenza espressa e le differenze genomiche tra gli ordini monocotiledoni asparagales e poale. Cellula vegetale 2004,16, 114-125. [CrossRef]
- 55. Kim, HJ; Lee, risorse umane; Hyun, JY; Canzone, KH; Kim, KH; Kim, JE; Hur, CG; Harn, CH Sviluppo di marcatori per test di purezza genetica della cipolla utilizzando SSR Finder. Razza J. coreana. Sci. 2012, 44, 421-432. [CrossRef]
- 56. Schuelke, M. Un metodo economico per l'etichettatura fluorescente dei frammenti di PCR. Naz. Biotecnologie. 2000, 18, 233-234. [CrossRef] [PubMed]
- 57. Peakall, R.; Smouse, PE GenAlEx 6.5: Analisi genetica in Excel. Software genetico delle popolazioni per l'insegnamento e la ricerca: un aggiornamento. Bioinformatica 2012, 28, 2537-2539. [CrossRef] [PubMed]
- 58. Kalinowski, ST; Conicità, ML; Marshall, TC La revisione del modo in cui il programma informatico CERVUS gestisce gli errori di genotipizzazione aumenta il successo nell'assegnazione della paternità. Mol. Eco. 2007,16, 1099-1106. [CrossRef]
- 59. Pritchard, JK; Stephens, M.; Rosenberg, Carolina del Nord; Donnelly, P. Mappatura dell'associazione in popolazioni strutturate. Sono. J. Hum. Genet. 2000, 67 170-181. [CrossRef]
- 60. Evanno, G.; Regnaut, S.; Goudet, J. Rilevamento del numero di gruppi di individui utilizzando il software STRUTTURA: uno studio di simulazione. Mol. Eco. 2005,14, 2611-2620. [CrossRef]
- 61. Conte, D.; VonHoldt, B. STRUCTURE HARVESTER: un sito Web e un programma per visualizzare l'output di STRUCTURE e implementare il metodo Evanno. Conserva. Genetta. Risorsa. 2011, 4. [CrossRef]
- 62. Takezaki, N.; Nei, M.; Tamura, K. POPTREEW: versione Web di POPTREE per costruire alberi di popolazione dai dati di frequenza allelica e calcolare alcune altre quantità. Mol. Biol. Evoluzione. 2014, 31 1622-1624. [CrossRef]
- 63. Kumar, S.; Stecher, G.; Li, M.; Knyaz, C.; Tamura, K. MEGA X. Analisi genetica evolutiva molecolare su piattaforme informatiche. Mol. Biol. Evoluzione. 2018, 35, 1547-1549. [CrossRef]